miten Potentiostaatti vaikuttaa (pähkinänkuoressa)?
kuten on mainittu ennen kuin potentiostaatti ohjaa työelektrodin potentiaalia ja mittaa sen läpi virtaavaa virtaa.
miksi ei vain kahta elektrodia? Yksi syy on, että emme voi mitata työelektrodin potentiaalia kiinteää pistettä vastaan, kun meillä on vain kaksi elektrodia.
Kuvittele kahden elektrodin järjestelmä, joka koostuu jo mainitusta työelektrodista ja elektrodista, minkä potentiaalin tulisi olla kiinteä vertailupisteemme, referenssielektrodi.
sovellamme tiettyä potentiaalia näiden elektrodien välillä ja sähkökemiallinen reaktio tapahtuu työelektrodilla, mutta koska piiri on suljettava ja virran on virrattava, reaktion, joka on käänteinen työelektrodilla tapahtuvalle reaktiolle, eli jos hapettuminen tapahtuu työelektrodilla, reduktion on tapahduttava referenssielektrodilla.
jos virta kulkee vakiopotentiaalilla, on sähkökemiallisen reaktion tapahduttava Faradayn lain mukaan:
yhtälö 3.1 / Faradayn laki
tämän yhtälön mukaan elektrodin läpi virtaava varaus Q on verrannollinen sellaisen lajin määrään n, joka otti tai antoi elektrodilla Z-elektroneja. F on Faradayn vakio ja edustaa 1 mol: n elektronien varausta. Virta I on varaus Q per aika t virtaa elektrodin läpi:
yhtälö 3.2
yhtälöt 3.1 ja 3.2 yhdistelmä osoittaa, että virtaava virta I liittyy elektrodissa tapahtuvaan reaktioon määrän n kautta:
yhtälö 3.3
Kuvittele nyt, että virta virtaa referenssielektrodin kohdalla. Tällä elektrodilla muunnetaan lajin määrä n. Tämä muunnos johtaa elektrodia ympäröivän liuoksen pinnan tai konsentraation muuttumiseen. Nernstin yhtälö osoittaa selvän korrelaation elektrodin potentiaalin E ja sen ympäröivän:

yhtälö 3.4 / Nernstin yhtälö
E0 on redox-parin Red And Ox standardipotentiaali. R on kaasuvakio ja T lämpötila. Lajin hapetetun ja pelkistyneen muodon AOX: n ja aredin aktiivisuutta ympäröivässä liuoksessa ei ole aina helppo ennustaa. Tämä johtaa usein yhtälön yksinkertaistamiseen:

yhtälö 3.5
kaksi aktiivisuuskerrointa fOx ja fRed sisältyvät tuloksena olevaan potentiaaliin E0′, jota kutsutaan formaaliksi potentiaaliksi. Koska se sisältää ympäristöstä riippuvia parametreja, kuten lämpötila-ja aktiivisuuskertoimia, E0′: tä ei voida luetella, mutta se on tarvittaessa määritettävä jokaista koetta varten. Useimmat analyyttisen kemian kokeet tehdään huoneenlämmössä (295 K). Tämä mahdollistaa uuden yksinkertaistamisen. Mukavuudesta myös ln siirretään lokiin.
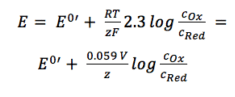
yhtälö 3.6
käytännön sovellutuksessa yhtälö 3.6 on Nernstin yhtälön käytetyin muoto. Monissa sovelluksissa voidaan olettaa, että E0 on suurin piirtein sama kuin E0′, koska molemmat aktiivisuuskertoimet ovat lähellä yhtä.
tässä muodossa (yhtälö 3.6) elektrodin ympäröivän ja sen potentiaalin välinen korrelaatio näkyy helpommin.
kuten mainittiin ennen kuin kaikki yhtälön 3.4 yksinkertaistukset suoritettiin: vertailuelektrodia ympäröivän liuoksen muuttuminen virtaavan virran vuoksi johtaa sen potentiaalin muuttumiseen, jonka oletetaan olevan kiinteä vertailupisteemme. Mutta emme voi rajoittaa virran virtausta referenssielektrodin (RE) läpi, koska kaikkien rajoitusten pitäisi johtua prosessista, jota haluamme tutkia, eli prosessista työelektrodilla (me).
ratkaisu tähän ongelmaan on kolmas elektrodi. Tällä laskurielektrodilla (CE), joka tunnetaan myös apuelektrodina, tapahtuu vastareaktio työelektrodin reaktioihin. Virta kulkee työ-ja laskurielektrodin välillä. Potentiaalia ohjataan työ – ja vertailuelektrodin välillä (KS.Kuva 3.1).

Kuva 3.1 / kaavamainen kolmen elektrodin järjestelmä
laskurin ja vertailuelektrodin välinen potentiaali säädetään siten, että työelektrodin läpi virtaava virta tietyssä potentiaalissa työ-ja vertailuelektrodin välillä täyttyy. Re: n ja WE: n (DC potential range) ja CE: n ja WE: n (compliance voltage) välillä voidaan soveltaa potentiaalisia a potentiostaatteja.
koska hallitset potentiaalia RE: n ja WE: n välillä, on helppo pysyä DC: n potentiaalialueen rajoissa. CE: n on oltava suurempi kuin me, koska käyttäjä ei voi ohjata vaatimustenmukaisuusjännitettä. Suurempi pinta samalla potentiaalilla johtaa suurempaan virtaan ja CE: n pitäisi tarjota tarpeeksi virtaa joutumatta vaatimustenmukaisuusjännitteeseen.
nyrkkisäännön mukaan CE: n tulisi olla 100 kertaa suurempi kuin WE: n. Monissa kokeissa tämä ei välttämättä ole tarpeen, mutta hyvän käytännön vuoksi kannattaa varmistaa, että CE on riittävän suuri, jotta se ei rajoita WE: ssä virtaavaa virtaa.
yleensä CE: n ja WE: n välinen etäisyys on riittävän suuri, joten näiden kahden elektrodin reaktiot eivät vaikuta toisiinsa, ja vastareaktio voidaan jättää huomiotta, mutta joskus, esimerkiksi pienissä määrissä, voi olla hyödyllistä tietää, mikä reaktio tapahtuu vastaelektrodissa.