Hvordan fungerer en Potentiostat (i en nøddeskal)?
som nævnt før styrer en potentiostat potentialet i arbejdselektroden og måler strømmen, der strømmer gennem den.
hvorfor ikke bare to elektroder? En af grundene er, at vi ikke kan måle potentialet i arbejdselektroden mod et fast punkt, når vi bare har to elektroder.
Forestil dig et toelektrodesystem, der består af den allerede nævnte arbejdselektrode og elektroden, hvilket potentiale skal være vores faste referencepunkt, referenceelektroden.
vi anvender et vist potentiale mellem disse elektroder, og der sker en elektrokemisk reaktion ved arbejdselektroden, men da kredsløbet skal lukkes, og strømmen skal strømme, skal der forekomme en reaktion, der er omvendt til reaktionen ved arbejdselektroden, det vil sige, hvis der opstår iltning ved arbejdselektroden, skal der ske en reduktion ved referenceelektroden.
hvis en strøm strømmer med et konstant potentiale, skal en elektrokemisk reaktion ske i henhold til Faradays lov:
ligning 3.1 / Faradays lov
denne ligning siger, at ladningen K, der strømmer gennem en elektrode, er proportional med mængden n af en art, der tog eller gav å-elektroner ved elektroden. F er Faraday konstant og repræsenterer ladningen af 1 mol elektroner. Den nuværende I er ladningen K pr. gang t, der strømmer gennem elektroden:
ligning 3.2
ligningerne 3.1 og 3.2 kombination viser, at den strøm, jeg strømmer, er forbundet med reaktionen, der sker ved elektroden via mængden n:
ligning 3.3
Forestil dig nu, at strømmen strømmer ved referenceelektroden. Ved denne elektrode omdannes en arts mængde n. Denne omdannelse fører til en ændring af overfladen eller koncentrationen af opløsningen omkring elektroden. Nernst-ligningen viser en klar sammenhæng mellem potentialet E for en elektrode og dens omgivende:

ligning 3.4 / Nernst ligning
E0 er standardpotentialet for redokseparret rød og okse. R er gas konstant og T temperaturen. Aktiviteten af den iltede og reducerede form af arten aoks og aRed i den omgivende opløsning er ikke altid let at forudsige. Dette fører ofte til en forenkling af ligningen:

ligning 3.5
de to aktivitetskoefficienter ræv og fRed er inkluderet i det resulterende potentiale E0′, som kaldes det formelle potentiale. Da det indeholder parametre, der afhænger af miljøet, såsom temperatur og aktivitetskoefficienter, kan E0′ ikke vises, men skal om nødvendigt bestemmes for hvert eksperiment. De fleste eksperimenter i analytisk kemi udføres ved stuetemperatur (295 K). Dette muliggør en anden forenkling. Af bekvemmelighed overføres også ln til loggen.
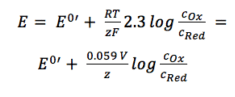
ligning 3.6
til praktisk anvendelse er ligning 3.6 den mest anvendte form for Nernst-ligningen. For mange applikationer kan man antage, at E0 er omtrent det samme som E0′, fordi begge aktivitetskoefficienter er tæt på en.
i denne form (ligning 3.6) er korrelationen mellem omgivelserne af en elektrode og dens potentiale lettere synlig.
som nævnt før blev alle forenklingerne ved ligning 3.4 udført: ændringen af opløsningen omkring referenceelektroden på grund af en strømningsstrøm fører til en ændring af potentialet, der formodes at være vores faste referencepunkt. Men vi kan ikke begrænse strømmen gennem referenceelektroden (RE), fordi alle begrænsninger skal være forårsaget af den proces, vi vil undersøge, det er processen ved arbejdselektroden (vi).
løsningen på dette problem er en tredje elektrode. Ved denne modelektrode (CE), også kendt som hjælpeelektroden, finder modreaktionen på arbejdselektrodens reaktioner sted. Strømmen strømmer mellem arbejds-og tællerelektroden. Potentialet styres mellem arbejds-og referenceelektroden (se figur 3.1).

figur 3.1 / et skematisk tre elektrodesystem
potentialet mellem tælleren og referenceelektroden justeres på en sådan måde, at strømmen, der strømmer gennem arbejdselektroden ved et bestemt potentiale mellem arbejds-og referenceelektroden, er opfyldt. Der er grænser for det potentiale, en potentiostat kan anvende mellem RE og vi (DC potential range) og CE og vi (compliance voltage).
da du styrer potentialet mellem RE og vi, er det let at holde sig inden for grænserne for DC potential range. CE skal være større end vi, fordi compliance spændingen ikke kan styres af brugeren. En større overflade med samme potentiale fører til en højere strøm, og CE skal give tilstrækkelig strøm uden at løbe ind i overholdelsesspændingen.
en tommelfingerregel antyder, at CE skal være 100 gange større end vi. For mange eksperimenter er dette muligvis ikke nødvendigt, men for en god praksis skal du sikre dig, at CE er stor nok, så den ikke begrænser strømmen, der strømmer ved vi.
normalt er afstanden mellem CE og vi stor nok, så reaktionerne fra de to elektroder ikke påvirker hinanden, og modreaktionen kan ignoreres, men nogle gange kan det i små mængder være nyttigt at vide, hvilken reaktion der sker ved tællerelektroden.