aan de muur hangen de vierkanten als een gekartelde muur van alfabet blokken. De letters vormen geen woorden. De kolommen zijn ongelijk. Deze grafiek – een icoon van de chemie-staat bekend als het Periodiek Systeem van de elementen. Dmitri Mendelejev( MEN-duh-LAY-ev), een Russische wetenschapper die in St.Petersburg werkt, kwam met een vroege versie. Dat was 150 jaar geleden. Maar zelfs vandaag de dag helpt deze grafiek wetenschappers om de atomen en moleculen te begrijpen die deel uitmaken van ons universum.
elementen zijn de bouwstenen van alle materie. Hun atomen breien samen om letterlijk alles te vormen-wij, de lucht die we inademen, de organismen die onze wereld delen en elk ander gasmolecuul Of beetje massa dat we in ons universum vinden.
de rijen en kolommen op het periodiek systeem geven de zogenaamde periodieke wet weer. Het stelt dat gedeelde eigenschappen tussen chemische elementen herhalen in regelmatige patronen als elementen groter worden. Deze patronen verbinden elementen met vergelijkbaar chemisch gedrag en helpen chemici te vertellen hoe atomen reageren om moleculen te vormen. Hoe de rijen en kolommen in deze tabel line-up wijst op gedeelde eigenschappen tussen groepen van gerelateerde elementen. Het begrijpen van die relaties helpt chemici nieuwe verbindingen te creëren. Het helpt hen ook te begrijpen hoe het leven werkt. Het helpt hen zelfs te voorspellen hoe nieuwe materialen zich zullen gedragen.

maar Mendelejev ‘ s bekende Horoscoop is verre van het enige periodiek systeem. Wetenschappers hebben er veel gebouwd, sommige met zeer verschillende vormen. Chemici hebben er een paar ontworpen. Wetenschappers en leraren op andere gebieden ontwikkelden anderen.”Alternate forms are useful because of the different aspects of the science that they illustrate,” notes Carmen Giunta. Hij is chemicus aan het Le Moyne College in Syracuse, N. Y. die minder traditionele periodieke tabellen bieden niet alleen manieren om een aantal van de eigenaardigheden van de chemie te benadrukken, zegt hij, maar ook om ze beter in beeld te brengen.
docenten en ouders, meld je aan voor het spiekbriefje
wekelijkse updates om je te helpen wetenschapsnieuws te gebruiken voor studenten in de leeromgeving
in 2019 viert de wereld het periodiek systeem in al zijn vormen en hoe het helpt de bouwstenen van ons universum te organiseren en te begrijpen.
het is elementair
vlak na de oerknal bestond het heelal uit alleen waterstof en helium — de twee lichtste elementen. Zwaartekracht bracht deze atomen samen in steeds grotere hoeveelheden. Uiteindelijk zou dit dichte, vurige hete ovens creëren die we kennen als sterren. In het centrum van deze sterren fuseerden intense druk atoomkernen — de centra van de atomen — waardoor grotere kernen ontstonden.
deze langzaam gesmeed Grotere en zwaardere elementen. Ze bevatten koolstof, een element dat essentieel is voor al het leven zoals wij het kennen. Die stellaire smederijen vormden ook de zuurstof die we nodig hebben om in te ademen.Het maken van elementen groter dan ijzer vereist nog meer kosmische vuurkracht. Zware atoomkernen gevormd als massieve, stervende sterren explodeerde. Deze supernova ‘ s sloegen met kracht kleinere elementen samen.Voor zijn periodiek systeem van 1869 rangschikte Mendelejev de elementen in volgorde van oplopende massa. Hij was een van de eerste wetenschappers die zich realiseerden dat chemie herhalingspatronen heeft. Naarmate elementen groter worden, herhalen sommige van hun eigenschappen zich uiteindelijk. Bepaalde elementen reageren liever en worden positief geladen. Sommigen zijn liever negatief geladen. Dergelijke patronen konden wetenschappers om te anticiperen of of hoe verschillende soorten elementen zou waarschijnlijk combineren.In zijn onderzoeksjournaal schreef Mendelejev dat het idee voor deze tabel in een droom tot hem kwam. Hij begon met een ruzie. Maar toen de chemische eigenschappen zich herhaalden, begon hij een nieuwe rij. Hij plaatste elementen met vergelijkbaar gedrag in kolommen. Hij liet gaten achter. Deze gaten, zo redeneerde hij, markeerden elementen die waarschijnlijk bestonden, maar nog niet ontdekt waren.Toen hij deze tabel publiceerde, voorspelde Mendelejev de eigenschappen en massa ‘ s van vier nieuwe elementen. Uiteindelijk werden alle vier ontdekt-drie binnen slechts 10 jaar.
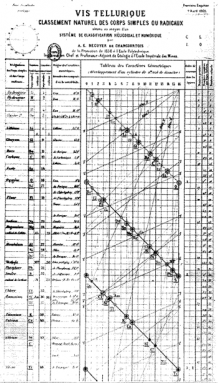
Alexandre-Émile Béguyer de Chancourtois was een Franse geoloog. Zeven jaar voor Mendelejev ‘ s beroemde tafel, creëerde hij een spiraal “tafel.”Hij rangschikte elementen in volgorde van atoomgewicht. Het toonde de herhalende periodes. Er waren echter geen onderbrekingen tussen de rijen. In plaats daarvan wondde hij zijn lange, dunne kaart rond een cilinder. Op deze manier, elke rij stroomde in de volgende. En soortgelijke elementen opgesteld boven elkaar in nette kolommen.
andere wetenschappers maakten vergelijkbare kaarten. Het duurde niet lang, inspanningen om alle bekende elementen te organiseren sneeuwbalde. Terwijl al deze grafieken evolueerden, steeg er één om te domineren. Het is vandaag de dag te zien in klaslokalen en schoolboeken over de hele wereld.
elk van de 118 bekende elementen heeft zijn eigen chemische symbool — een of twee letters die trots de naam van het element vertegenwoordigen uit zijn doos op het periodiek systeem. Sommige van deze afkortingen zijn duidelijk, zoals H voor waterstof of C voor koolstof. Andere dateren uit de oudheid. Het symbool van natrium is bijvoorbeeld Na. Waarom? In het Latijn heet natrium natrium.
elk vak op de tabel heeft een heel getal, meestal in de linkerbovenhoek. Het heet het atoomnummer, het geeft aan hoeveel protonen, of positief geladen deeltjes, zijn verpakt in de kern van het element. Die kern omvat ook neutronen (deeltjes met massa maar zonder lading). Rondom de kern bevindt zich een wolk van veel kleinere, negatief geladen elektronen.
het onderste getal in het vierkant van de grafiek bevat voor elk element cijfers na een komma. Deze waarde is de atoommassa van het element. Het vertegenwoordigt de gemiddelde massa van een atoom van dat element.
het periodiek systeem is eenvoudig, krachtig en blijft nieuwe experimenten opleveren, zegt Eric Scerri. Hij doceert scheikunde aan de Universiteit van Californië, Los Angeles. Hij schrijft ook boeken over het periodiek systeem. Hij beschrijft de organiserende principes achter het periodiek systeem als “een absoluut belangrijke ontdekking.”
Dual towers domineerden
het meest voorkomende periodiek systeem van vandaag wordt ook wel de “twin towers” versie genoemd. Waterstof (H) kroont de hoge toren aan de linkerkant. Helium (He) boven de rechter toren.

naarmate atomen groter worden, worden ze complexer. In deze grafieken verwijst een periode binnen het periodiek systeem naar een Rij elementen die een herhalende cyclus vertonen. Binnen de tabel wordt de breedte van een Rij — ook wel een periode genoemd — bepaald zodat het patroon van het gedrag van elementen binnen een kolom wordt gehandhaafd. Het patroon herhaalt zich eerst in twee elementen, zodat de rij twee elementen breed is. Dan herhaalt het patroon zich in acht elementen. En als de elementen groter worden, merkt Scerri op :” de perioden worden langer en langer — – uiteindelijk met 18 elementen, en dan 32.
de langere, Grotere perioden kunnen de basis van zware elementen van deze tabel onhandig breed maken. Om dit te omzeilen, de Twin tower grafiek trekt meestal een deel van de onderste twee rijen. Het plaatst deze elementen onderaan de pagina, bijna als voetnoten. Deze onderste rijen bevatten groepen van elementen die bekend staan als de lanthaniden (LAN-tha-nydes) en actiniden (AK-tih-nydes).
actiniden bevatten de nieuwste en grootste elementen. Velen zijn radioactief en komen niet van nature voor. Natuurkundigen maken ze in laboratoria door kleinere elementen in elkaar te bombarderen. Deze radioactieve, superzware elementen zijn ook super onstabiel. Dat betekent dat ze uiteenvallen in kleinere elementen binnen fracties van een seconde.
hoe ze nuttig zijn
een periodiek systeem kan dienen als een soort receptenboek. De grafiek laat zien hoe elementen zich tot elkaar verhouden. Dus waar een element op de tafel zit vertelt een chemicus hoe het wel of niet kan interageren met andere ingrediënten. Vaak omvatten deze nuttige eigenschappen de massa, het kookpunt en andere belangrijke gegevens.
de tabel helpt chemici problemen op te lossen. Chemici zouden bijvoorbeeld een nieuwe verbinding willen maken met eigenschappen die vergelijkbaar zijn met een bestaande — gewoon beter. Dus ze zouden kunnen zoeken naar een vervanger met soortgelijke functies, te beginnen met een ander element uit dezelfde kolom op de tafel.Het echte geschenk van deze tabellen, zegt Brigitte van Tiggelen, is “alle informatie op één plaats te hebben en te onderwijzen en te delen.”Als historicus werkt ze als Europees directeur voor het Science History Institute in Philadelphia, Pa.
De Twin tower chart heeft vele voordelen, zegt Mark Leach. Hij is chemicus in Engeland aan de Manchester Metropolitan University. Geen enkele andere tabel slaagt erin om de herhalende patronen zo goed te laten zien, betoogt hij, al die tijd met inbegrip van andere functies.
bijvoorbeeld, alle metalen bevinden zich aan de linkerkant. Niet-metalen hangen aan de rechterkant. Deze grafiek laat ook zien hoe de grootte van een atoom verandert en hoe gemakkelijk het waarschijnlijk een elektron zal opgeven. Dergelijke eigenschappen zijn belangrijk om te begrijpen hoe atomen zullen handelen, reageren en trouwen met anderen om moleculen te vormen.

maar de Twin towers kaart is niet perfect.
chemici ruziën vaak over de plaats waar bijvoorbeeld waterstof en helium moeten worden geplaatst. En een platte, tweedimensionale tabel laat niet echt zien hoe de rijen met elkaar verbonden zijn. Als je aan het einde van een rij komt, zegt Scerri: “je krijgt het gevoel dat je er een beetje vanaf valt.”
Roy Alexander werkte als tentoonstellingsbouwer. Hij vond het niet leuk hoe de rijen van de twin tower tafel abrupt eindigden. Dus in 1965 sneed hij een traditionele periodieke tabel in strips. Daarna zette hij ze weer in elkaar en creëerde een 3D-versie.Jaren later ontdekte hij dat de natuurkundige George Gamow in de jaren 1940 een vrijwel identieke tabel bouwde. Herinnert Alexander zich: “het was verbazingwekkend hoe identiek het leek op mijn patenttekening.”
rekening houdend met de steeds grotere perioden
toen Béguyer de Chancourtois voor het eerst zijn periodiek systeem creëerde, waren veel van de grootste elementen nog niet ontdekt. Naarmate de elementen groter worden, herhalen de gedeelde kenmerken zich minder vaak. Uiteindelijk, de langere rijen met de Lanthanide en actinide elementen maakte de traditionele grafiek onhandig breed.
in een 3D-tabel kunnen deze langere rijen worden opgenomen door de spiraal gewoon breder te maken. De Canadese chemicus Fernando Dufour ontwierp ElemenTree om dit te illustreren (zie foto). Hij maakte elke periode als een zeshoekige laag die alle elementen die meestal zou verschijnen in een enkele rij op de twin-tower grafiek bevatte. Soortgelijke elementen staan nog steeds verticaal.

maar een boomvormige tafel is niet het enige 3D-antwoord. In de jaren 50 vertrouwde scheikundeleraar Jennie Clauson op een cilinder voor haar tafel. Maar in plaats van uitpuilende extra elementen, stopte ze een aantal van hen naar het midden.
een ander probleem met de twin tower tafel is waar waterstof en helium moeten worden geplaatst. Waterstof werkt soms meer als een metal, bijvoorbeeld. Het zal zijn elektron verliezen en negatief geladen ionen aantrekken. Andere keren werkt het als een niet-metaal en grijpt een extra elektron en wordt negatief geladen. Dan werkt het meer als een fluor of chloor en sponzen positieve ionen.Om dit te verklaren creëerde chemicus Theodor Benfey in de jaren zestig een vlakke spiraaltafel die waterstof en helium in het midden van een grote blauwe cirkel plaatste. Elk van de drie buitenste spaken binnen de cirkel vertegenwoordigt een groep van soortgelijke elementen. Om de grotere elementen en de groeiende periodieke cycli op te nemen, voegde hij terrassen toe die uitstulpen uit de cirkel. Zij omvatten de overgangsmetalen, lanthanides en actinides.
een platte tafel zoals de twin towers is handig om aan de muur te hangen of om in een boek te drukken. Leach voegt echter toe: “Er is echt geen reden waarom het periodiek systeem niet driedimensionaal is.”
plezier en spelletjes?
een van de meest recente toevoegingen aan de groeiende bibliotheek van periodieke tabellen is afkomstig van de European Chemical Society, of ECS. ECS is gevestigd in Brussel, België en heeft als doel de aandacht te vestigen op de relatieve schaarste van veel belangrijke elementen. Het merkt op dat 30 elementen gaan in het maken van een typische mobiele telefoon. En veel van die elementen zijn niet op grote schaal beschikbaar.
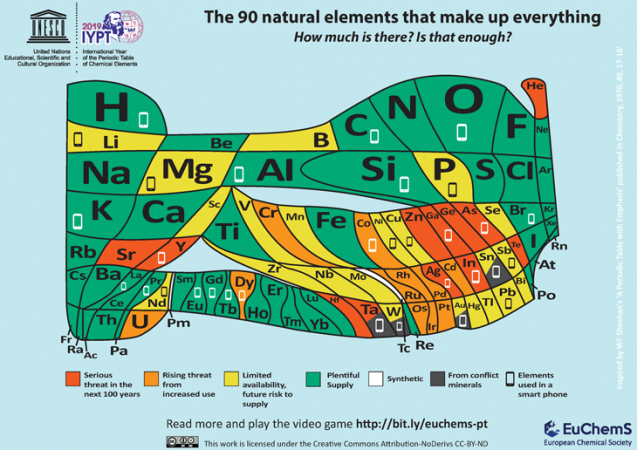
“de noodzaak om zorgvuldig te kijken naar onze neiging om afval en onjuist recyclen van dergelijke items,” de ECS betoogt. “Tenzij er oplossingen worden geboden, lopen we het risico dat veel van de natuurlijke elementen die deel uitmaken van de wereld om ons heen opraken — of het nu gaat om beperkte voorraden, hun locatie in conflictgebieden of ons onvermogen om ze volledig te recyclen.”
het ECS erkent dat deze nieuwe tabel “tot nadenken stemt.”En dat is geen toeval. Het wil dat mensen de waarde begrijpen van het niet verspillen van “bedreigde elementen.”Iedereen, zegt het, moet” zich afvragen of upgrades naar onze telefoons en andere elektronische apparaten echt nodig zijn.”En als onze elektronica afsterft, zegt het: “we moeten ervoor zorgen dat we recyclen” zodat relatief schaarse elementen “niet op stortplaatsen terechtkomen of het milieu vervuilen.”
om te onderzoeken hoe mensen elementen gebruiken, heeft de ECS een gratis online videospel ontwikkeld: Elementary Escapades.
er is genoeg ruimte voor meer nieuwe periodieke tabellen, zegt Leach in Manchester. In feite heeft hij een hobby gemaakt van het verzamelen van nieuwe en ze online te plaatsen. Hij is ook altijd op zoek naar oude. “Ik krijg waarschijnlijk elke week een nieuwe”, zegt hij.Scerri heeft studenten ook nieuwe laten ontwikkelen. “Ieder, “zegt hij,” heeft een kleine deugd van zijn eigen.”